Por que alguns tumores se espalham enquanto outros permanecem localizados? Os cientistas ainda não compreendem completamente o que controla a capacidade de metástase de uma célula cancerígena, mas responder a esta questão é essencial para melhorar o atendimento ao paciente. Pesquisadores da Universidade de Genebra (UNIGE) estudaram células do câncer de cólon e identificaram fatores-chave que influenciam a probabilidade de um tumor se espalhar. Eles também descobriram padrões específicos de expressão genética que podem ser usados para estimar esse risco.
Com base nestas descobertas, a equipa desenvolveu uma ferramenta de inteligência artificial (MangroveGS) que converte estes sinais genéticos em previsões altamente fiáveis em vários tipos de cancro. O estudo, publicado em Relatórios de célulaspoderia levar a tratamentos mais personalizados e ajudar a descobrir novos alvos terapêuticos.
Câncer como um processo de desenvolvimento distorcido
“A origem do cancro é frequentemente atribuída a ‘células anárquicas’”, explica Ariel Ruiz i Altaba, professor do Departamento de Medicina Genética e Desenvolvimento da Faculdade de Medicina da UNIGE, que liderou o estudo. “No entanto, o câncer deveria ser entendido como uma forma distorcida de desenvolvimento.” Mudanças genéticas e epigenéticas podem reativar programas biológicos que normalmente são desligados após o desenvolvimento inicial, levando, em última análise, à formação de tumores.
Em vez de ser aleatório, o cancro parece seguir regras biológicas estruturadas. “O desafio é, portanto, encontrar as chaves para compreender a sua lógica e forma. E, no caso das metástases, identificar as características das células que se separarão do tumor para criar outro noutro local do corpo”.
Rastreamento de células cancerígenas metastáticas
A metástase é responsável pela maioria das mortes por câncer, especialmente nos cânceres de cólon, mama e pulmão. No momento em que as células cancerígenas são detectadas circulando no sangue ou no sistema linfático, a doença muitas vezes já começou a se espalhar. Embora os cientistas compreendam muitas das mutações que levam à formação de tumores, nenhuma alteração genética explica por que algumas células se separam e migram enquanto outras permanecem no lugar.
“A dificuldade reside em poder determinar a identidade molecular completa de uma célula – uma análise que a destrói – enquanto se observa a sua função, que exige que ela permaneça viva”, explica o professor Ruiz i Altaba. Para superar isso, os pesquisadores isolaram, clonaram e cultivaram células tumorais em laboratório. “Esses clones foram então avaliados in vitro e em modelo de camundongo para observar sua capacidade de migrar através de um filtro biológico real e gerar metástases”, acrescenta Arwen Conod.
Assinaturas genéticas ligadas à propagação do câncer
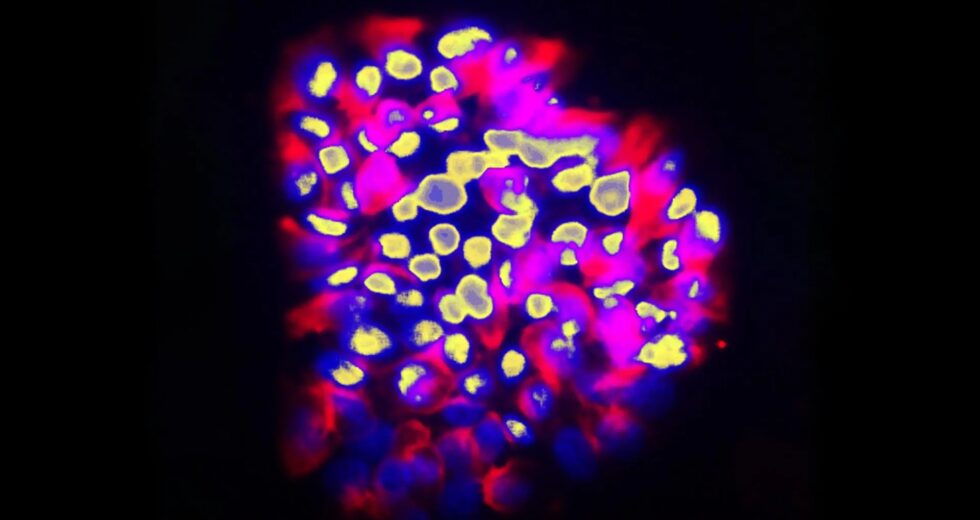
A equipe analisou a atividade de centenas de genes em cerca de trinta clones de células retirados de dois tumores primários do cólon. Isto revelou padrões claros de expressão genética que correspondiam de perto à capacidade de cada célula se mover e se espalhar. É importante ressaltar que o potencial metastático não foi determinado pelo perfil de uma única célula, mas pela forma como grupos de células cancerígenas relacionadas interagem entre si.
Ferramenta de IA prevê risco de metástase
Os pesquisadores integraram essas assinaturas genéticas em um sistema de inteligência artificial. “A grande novidade da nossa ferramenta, chamada ‘Mangrove Gene Signatures (MangroveGS)’, é que ela explora dezenas, até centenas, de assinaturas genéticas. Isso a torna particularmente resistente a variações individuais”, explica Aravind Srinivasan.
Após o treinamento, o modelo foi capaz de prever metástases e recorrência do câncer de cólon com quase 80% de precisão, superando os métodos existentes. As mesmas assinaturas genéticas derivadas do câncer de cólon também se mostraram úteis na previsão do risco metastático em outros tipos de câncer, incluindo câncer de estômago, pulmão e mama.
Rumo a um tratamento mais personalizado do câncer
O MangroveGS pode trabalhar diretamente com amostras de tumores coletadas em hospitais. As células são analisadas, seu RNA é sequenciado e uma pontuação de risco de metástase é rapidamente gerada e compartilhada de forma segura com médicos e pacientes por meio de uma plataforma criptografada.
“Essa informação evitará o tratamento excessivo de pacientes de baixo risco, limitando assim os efeitos colaterais e os custos desnecessários, ao mesmo tempo que intensificará o monitoramento e o tratamento daqueles de alto risco”, afirma Ariel Ruiz i Altaba. “Também oferece a possibilidade de otimizar a seleção de participantes em ensaios clínicos, reduzindo o número de voluntários necessários, aumentando o poder estatístico dos estudos e proporcionando benefícios terapêuticos aos pacientes que mais necessitam”.